অ্যামোনিয়াম ডাইহাইড্রোজেন ফসফেট
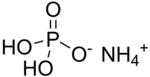
অ্যামোনিয়াম ডাইহাইড্রোজেন ফসফেট (এডিপি) একটি রাসায়নিক যৌগ। এটি মনোঅ্যামোনিয়াম ফসফেট ( এমএপি ) নামেও পরিচিত।[৫] এটির রাসায়নিক সংকেত (NH4)(H2PO4)। এটি কৃষি সার[৬] এবং শুষ্ক রাসায়নিক অগ্নি নির্বাপক যন্ত্রের একটি প্রধান উপাদান। আলোকবিদ্যা [৭] এবং ইলেকট্রনিক্সেও এর উল্লেখযোগ্য ব্যবহার রয়েছে। [৮]

| |
| |

| |
| নামসমূহ | |
|---|---|
| ইউপ্যাক নাম
অ্যামোনিয়াম ডাইহাইড্রোজেন ফসফেট
| |
| অন্যান্য নাম
মনোঅ্যামোনিয়াম ফসফেট
| |
| শনাক্তকারী | |
ত্রিমাত্রিক মডেল (জেমল)
|
|
| সিএইচইবিআই | |
| কেমস্পাইডার | |
| ইসিএইচএ ইনফোকার্ড | ১০০.০২৮.৮৭৭ |
| ইসি-নম্বর |
|
| ই নম্বর | E৩৪২(i) (অ্যান্টিঅক্সিডেন্ট, ...) |
পাবকেম CID
|
|
| ইউএনআইআই | |
কম্পটক্স ড্যাশবোর্ড (EPA)
|
|
| |
| |
| বৈশিষ্ট্য | |
| H6NO4P | |
| আণবিক ভর | ১১৫.০২ g·mol−১ |
| বর্ণ | সাদা স্ফটিকস্বরূপ |
| গন্ধ | নেই |
| ঘনত্ব | ১.৮ গ্রা/সেমি৩ |
| গলনাঙ্ক | ১৯০ °সে (৩৭৪ °ফা; ৪৬৩ K) |
| (গ্রা/ডিএল) ২৮ (১০ °সে) ৩৬ (২০ °সে) ৪৪ (৩০ °সে) 56 (৪০ °সে) ৬৬ (৫০ °সে) ৮১ (৬০ °সে) ৯৯ (৭০ °সে) ১১৮ (৮০ °সে) ১৭৩ (১০০ °সে)[২][৩] | |
| দ্রাব্যতা | ইথানলে অদ্রবণীয়[২] অ্যাসিটোনে অদ্রবণীয় |
| প্রতিসরাঙ্ক (nD) | ১.৫২৫ |
| গঠন | |
| স্ফটিক গঠন | টেট্রাগোনাল |
| তাপ রসায়নবিদ্যা | |
| গঠনে প্রমান এনথ্যাল্পির পরিবর্তন ΔfH |
−১৪৪৫.০৭ কিলোজুল/মোল[৪] |
| ঝুঁকি প্রবণতা | |
| জিএইচএস চিত্রলিপি | 
|
| জিএইচএস সাংকেতিক শব্দ | সতর্কতা |
| জিএইচএস বিপত্তি বিবৃতি | H319 |
| জিএইচএস সতর্কতামূলক বিবৃতি | P261, P264, P271, P280, P302+352, P304+340, P305+351+338, P312, P321, P332+313, P337+313, P362, P403+233, P405 |
| এনএফপিএ ৭০৪ | |
| প্রাণঘাতী ডোজ বা একাগ্রতা (LD, LC): | |
LD৫০ (মধ্যমা ডোজ)
|
৫৭৫০ মিগ্রা/কেজি (rat, oral) |
| সম্পর্কিত যৌগ | |
অন্যান্য অ্যানায়নসমূহ
|
অ্যামোনিয়াম ফসফেট ডাইঅ্যামোনিয়াম ফসফেট |
অন্যান্য ক্যাটায়নসমূহ
|
মনোসোডিয়াম ফসফেট পটাশিয়াম ডাইহাইড্রোজেন ফসফেট |
সুনির্দিষ্টভাবে উল্লেখ করা ছাড়া, পদার্থসমূহের সকল তথ্য-উপাত্তসমূহ তাদের প্রমাণ অবস্থা (২৫ °সে (৭৭ °ফা), ১০০ kPa) অনুসারে দেওয়া হয়েছে। | |
| তথ্যছক তথ্যসূত্র | |
রাসায়নিক বৈশিষ্ট্য
সম্পাদনামনোঅ্যামোনিয়াম ফসফেট পানিতে দ্রবণীয় এবং এটি থেকে টেট্রাগোনাল পদ্ধতিতে অ্যানহাইড্রাস লবণ হিসাবে দীর্ঘায়িত প্রিজম বা সূঁচ হিসাবে স্ফটিক করে।[৭] এটি ইথানলে কার্যত অদ্রবণীয়।[২]
কঠিন মনোঅ্যামোনিয়াম ফসফেটকে পরীক্ষণে ২০০ ডিগ্রি সেলসিয়াস তাপমাত্রা পর্যন্ত স্থিতিশীল হিসাবে বিবেচনা করা যেতে পারে। এটি বিয়োজিত হয়ে অ্যামোনিয়া NH
3 এবং গলিত ফসফরিক এসিড H
3PO
4 উৎপন্ন হয়।
[৯] ১২৫ °সে এ অ্যামোনিয়ার আংশিক চাপ ০.০৫ মিমি পারদ হয়।[১০]
স্টকিয়মেট্রিক মনোঅ্যামোনিয়াম ফসফেটের দ্রবণ হল অম্লীয় (পিএইচ ৪.৭, ০.১% ঘনত্বে, ৪.২ এ ৫%)।[১১]
প্রস্তুতি
সম্পাদনামনোঅ্যামোনিয়াম ফসফেট সঠিক অনুপাতে ফসফরিক অ্যাসিড এবং অ্যামোনিয়ার তাপোৎপাদী বিক্রিয়া দ্বারা শিল্পে প্রস্তুত করা হয়: [১২]
NH
3 + H
3PO
4 → NH
4H
2PO
4
অবস্থান
সম্পাদনাযৌগটি প্রকৃতিতে বিরল খনিজ বাইফসফামাইট হিসাবে উপস্থিত রয়েছে।
ব্যবহার
সম্পাদনাকৃষি
সম্পাদনামনোঅ্যামোনিয়াম ফসফেটের সবচেয়ে বেশি ব্যবহার কৃষিতে, সারের উপাদান হিসাবে। এটি হতে উদ্ভিদ ব্যবহারযোগ্য আকারে নাইট্রোজেন এবং ফসফরাস মাটি হতে শোষণ করে। এর এনপিকে লেবেল হলো ১২-৬১-০ (১২-২৭-০), যার অর্থ এটিতে মৌলিক নাইট্রোজেন ১২% এবং ফসফরাস পেন্টক্সাইড P
2O
5 ৬১% বা মৌলিক ফসফরাস ২৭% বিদ্যমান।
অগ্নি নির্বাপক
সম্পাদনাযৌগটি কিছু শুকনো রাসায়নিক অগ্নি নির্বাপক যন্ত্রে এবিসি পাউডারের একটি উপাদান।
আলোকবিজ্ঞান
সম্পাদনামনোঅ্যামোনিয়াম ফসফেট তার বায়ারফ্রিঞ্জেন্স বৈশিষ্ট্যের কারণে অপটিক্সের ক্ষেত্রে একটি বহুল ব্যবহৃত স্ফটিক। এর টেট্রাগোনাল স্ফটিক গঠনের ফলে, এই উপাদানটির নেতিবাচক অক্ষীয় অপটিক্যাল প্রতিসাম্য রয়েছে। এটির সাধারণত অপটিক্যাল তরঙ্গদৈর্ঘ্যে no = 1.522 এবং ne = 1.478 প্রতিসরাঙ্ক রয়েছে। [৭]
ইলেকট্রনিক্স
সম্পাদনামনোঅ্যামোনিয়াম ফসফেট স্ফটিকগুলি পাইজোইলেক্ট্রিক, কিছু সক্রিয় সোনার (SONAR) ট্রান্সডুসারের জন্য প্রয়োজনীয় একটি বৈশিষ্ট্য। ১৯৫০-এর দশকে এডিপি স্ফটিকগুলি মূলত ট্রান্সডিউসারগুলিতে কোয়ার্টজ এবং রোচেল সল্ট স্ফটিকগুলির পরিবর্তে ব্যবহার শুরু হয়েছিল। [৮]
খেলনা
সম্পাদনাতুলনামূলকভাবে বিষাক্ত নয় বলে এমএপি বিনোদন মূলক ব্যবহারের ক্ষেত্রে জনপ্রিয় পদার্থ। এটি বিভিন্ন রঙের রঞ্জক মিশ্রিত খেলনা কিট হিসাবে বিক্রি করা হয়।
তথ্যসূত্র
সম্পাদনা- ↑ Lide, David R. (১৯৯৮)। Handbook of Chemistry and Physics (87 সংস্করণ)। Boca Raton, Florida: CRC Press। পৃষ্ঠা 4–40। আইএসবিএন 0-8493-0594-2।
- ↑ ক খ গ Dejun Xu, Xing Xiong, Lin Yang, Zhiye Zhang, and Xinlong Wang (2016): "Determination of the Solubility of Ammonium Dihydrogen Phosphate in Water-Ethanol System at Different Temperatures from 283.2 to 343.2 K".
- ↑ Chemical Book: "Ammonium dihydrogen phosphate". Accessed on 2018-08-14.
- ↑ National Bureau of Standards. Selected Values of Chemical Thermodynamic Properties. Technical note 270-3. 1968 [১]
- ↑ "Monoammonium Phosphate (MAP)" (পিডিএফ)। www.mosaicco.com। ১৭ নভেম্বর ২০১৫ তারিখে মূল (পিডিএফ) থেকে আর্কাইভ করা। সংগ্রহের তারিখ ২০১৫-০৬-০৫।
- ↑ IPNI। "Monoammonium Phosphate (MAP)" (পিডিএফ)। www.ipni.net। International Plant Nutrition Institute। সংগ্রহের তারিখ ২১ জুলাই ২০১৪।
- ↑ ক খ গ Amnon Yariv, Pochi Yeh (১৯৮৪)। Optical Waves in Crystals। Wiley, Inc।
- ↑ ক খ Willem Hackmann (১৯৮৪)। Seek and Strike: Sonar, Anti-Submarine Warfare and the Royal Navy, 1914–1954। Her Majesty's Stationery Office। আইএসবিএন 0-11-290423-8।
- ↑ G. O. Guerrant and D. E. Brown (196): "Thermal Decomposition of High-Analysis Fertilizers Based on Ammonium Phosphate".
- ↑ John R Van Wazer (১৯৫৮)। Phosphorus And Its Compounds - Volume I: Chemistry। Interscience Publishers, Inc। পৃষ্ঠা 503।
- ↑ Haifa Chemicals Ltd.: "Mono-Ammonium Phosphate 12-61-0 ওয়েব্যাক মেশিনে আর্কাইভকৃত ১৫ অক্টোবর ২০২২ তারিখে".
- ↑ Martin Bäckman, Martin Gunnarsson, Linnea Kollberg, Martin Müller, and Simon Tallvod (2016): "Production of Monoammonium Phosphate at Yara AB ওয়েব্যাক মেশিনে আর্কাইভকৃত ১৮ নভেম্বর ২০১৭ তারিখে".
