অ্যাডিনোসিন ট্রাইফসফেট
এই নিবন্ধটি অন্য একটি ভাষা থেকে আনাড়িভাবে অনুবাদ করা হয়েছে। এটি কোনও কম্পিউটার কর্তৃক অথবা দ্বিভাষিক দক্ষতাহীন কোনো অনুবাদক কর্তৃক অনূদিত হয়ে থাকতে পারে। |
অ্যাডেনোসিন ট্রাইফোসফেট ( এটিপি ) একটি জৈব যৌগ যা জীবিত কোষকে বিভিন্ন প্রক্রিয়া চালিত করার জন্য শক্তি সরবরাহ করে । যেমন বলতে পারি পেশী সংকোচন, স্নায়ু প্রবণতা বর্ধন এবং রাসায়নিক সংশ্লেষণ সবই অ্যাডেনোসিন ট্রাইফোসফেটের জন্য হয়। জীবনে সকল রূপে পাওয়া এটিপি প্রায়শই অন্তঃকোষীয় শক্তি স্থানান্তরের জন্য জৈব মুদ্রা হিসাবে পরিচিত।[২][৩] বিপাকীয় প্রক্রিয়াতে ভাঙ্গলে বা গ্রাস করলে এটি অ্যাডিনোসিন ডিফোসফেট (এডিপি) বা অ্যাডেনোসিন মনোফসফেট (এএমপি) রূপান্তর করে। অন্যান্য প্রক্রিযইয়াতে এটিপি পুনরুত্থিত করে যাতে মানব শরীর প্রতি দিন এটিপিতে তার নিজের দেহের ওজনের সমতুল্য পুনর্ব্যবহার করে। [৪] এটি ডিএনএ এবং আরএনএর পূর্বসূরী এবং কোএনজাইম হিসাবে ব্যবহৃত হয়।
| |
| শনাক্তকারী | |
|---|---|
ত্রিমাত্রিক মডেল (জেমল)
|
|
| সিএইচইবিআই | |
| সিএইচইএমবিএল | |
| কেমস্পাইডার | |
| ড্রাগব্যাংক | |
| ইসিএইচএ ইনফোকার্ড | ১০০.০০০.২৫৮ |
| ইসি-নম্বর | |
| কেইজিজি | |
পাবকেম CID
|
|
| ইউএনআইআই | |
কম্পটক্স ড্যাশবোর্ড (EPA)
|
|
| |
| |
| বৈশিষ্ট্য | |
| C10H16N5O13P3 | |
| আণবিক ভর | 507.18 g/mol |
| ঘনত্ব | ১.০৪ গ্রা/সেন্টি৩ (disodium salt) |
| গলনাঙ্ক | ১৮৭ °সে (৩৬৯ °ফা; ৪৬০ K) disodium salt; decomposes |
| অম্লতা (pKa) | 6.5 |
| λmax | 259 nm[১] |
| পরিশোষণ | ε259 = 15.4 mM−1 cm−1 [১] |
সুনির্দিষ্টভাবে উল্লেখ করা ছাড়া, পদার্থসমূহের সকল তথ্য-উপাত্তসমূহ তাদের প্রমাণ অবস্থা (২৫ °সে (৭৭ °ফা), ১০০ kPa) অনুসারে দেওয়া হয়েছে। | |
| তথ্যছক তথ্যসূত্র | |
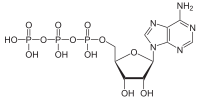
জৈব রসায়নের দৃষ্টিকোণ থেকে এটিপিকে নিউক্লিওসাইড ট্রাইফসফেট হিসাবে শ্রেণীবদ্ধ করা হয। যা নির্দেশ করে যে এটি তিনটি উপাদান নিয়ে গঠিত: একটি নাইট্রোজেনাস বেস ( অ্যাডেনিন ), চিনি রাইবোজ এবং ট্রাইফোফেট ।
গঠন
সম্পাদনাএর গঠনের দিক থেকে, এটিপিতে একটি চিনির ( রাইবোস ) ১ ′ কার্বন পরমাণুর সাথে ৯-নাইট্রোজেন পরমাণু দিয়ে সংযুক্ত একটি অ্যাডেনিন থাকে। এটি ঘুরে ফিরে চিনির ৫ 'কার্বন পরমাণুকে একটি ট্রাইফসফেট গ্রুপের সাথে সংযুক্ত করে। বিপাক সম্পর্কিত এর অনেকগুলি প্রতিক্রিয়ার মধ্যে অ্যাডেনিন এবং চিনির গ্রুপগুলি অপরিবর্তিত রয়েছে। তবে ট্রাইফোসফেটটি যথাক্রমে ডেরিভেটিভস এডিপি এবং এএমপি দিয়ে ডিআই এবং মনোফসফেটে রূপান্তরিত হয়। তিনটি ফসফরিল গ্রুপকে আলফা (α), বিটা (β), এবং টার্মিনাল ফসফেট গামা (γ) হিসাবে উল্লেখ করা হয়।
নিরপেক্ষ সমাধানে আয়নযুক্ত এটিপি বেশিরভাগই এটিপি৪− হিসাবে উপস্থিত রয়েছে এবং এটিপি ৩− এর একটি স্বল্প অনুপাত সহ। [৫]
এটিপিতে ধাতব কেশনগুলি বাঁধাই
সম্পাদনাপলিয়িনিয়নিক হওয়া এবং একটি সম্ভাব্য চিটলেটযোগ্য পলিফোসফেট গ্রুপের বৈশিষ্ট্যযুক্ত, এটিপি উচ্চ শখ্যতার সাথে ধাতব কেশনগুলিকে আবদ্ধ করে। Mg
২+ জন্য বাধ্যতামূলক ধ্রুবক Mg
২+ ( ৯ ৫৫৪ )। [৬] প্রায়শই সবসময় ম্যাগনেসিয়াম একটি যোজনী আয়নের বন্ধন বিভিন্ন প্রোটিনের সাথে এটিপি'র মিথস্ক্রিয়াকে দৃঢ়ভাবে প্রভাবিত করে। এটিপি- Mg২+ মিথস্ক্রিয়তার শক্তির কারণে Mg
২+ সাথে জটিল হিসাবে বেশিরভাগ ক্ষেত্রে কোষে এটিপি বিদ্যমান থাকে Mg
২+ ফসফেট অক্সিজেন কেন্দ্রগুলিতে বন্ধনে আবদ্ধ। [৫][৭]
কিনেজ ডোমেইনে এটিপি বাইন্ডিংয়ের জন্য দ্বিতীয় ম্যাগনেসিয়াম আয়নটি সমালোচিত। [৮] Mg ২+ এর উপস্থিতি কিনাস ক্রিয়াকলাপ নিয়ন্ত্রণ করে। [৯]
রাসায়নিক বৈশিষ্ট্য
সম্পাদনাপিএইচ এর জলীয় দ্রবণে এটিপির স্থিতিশীল ৬.৮ এবং অনুঘটক অনুপস্থিতিতে ৭.৪। আরো চরম পিএইচএসে এটি এডিপি এবং ফসফেটে দ্রুত হাইড্রোলাইজ হয়। জীবিত কোষগুলি এডিপির ঘনত্বের চেয়ে পাঁচগুণ বেশি এটিপি ঘনত্বের সাথে ভারসাম্য থেকে দশ দশমিক বেশি এটিপি-র এডিপির অনুপাত বজায় রাখে। [১০][১১] জৈব রাসায়নিক বিক্রিয়াগুলির প্রসঙ্গে POP বন্ধন প্রায়শই উচ্চ-শক্তি বন্ধন হিসাবে উল্লেখ করা হয়। [১২] এডিপি এবং অজৈব ফসফেটের মধ্যে এটিপি হাইড্রোলাইসিস ৩০.৫ প্রকাশ করে ৩.৪ এর থার্মোডাইনামিক মুক্ত শক্তি পরিবর্তনের সাথে এনজেপলির তিল প্রতি জোলে কিলোজুল / মোল। [১৩] ১ টি ভালো অবস্থায় এটিপি থেকে ফসফেট (Pi ) বা পাইরোফসফেট (PP i ) ইউনিট ক্লিভ করে শক্তি নির্গত হয় এম হলেন:[১৪]
- ATP + H
2O
H
2O → ADP + P i Δ জি ° = −30.5 কেজি / মল (.৩৭.৩ কিলোক্যালরি / মোল) - ATP + H
2O
H
2O → AMP + PP i Δ জি ° = −45.6 কেজি / মল (−10.9 কিলোক্যালরি / মোল)
এই সংক্ষিপ্ত সমীকরণ আরও স্পষ্টভাবে লেখা যেতে পারে (আর = অ্যাডিনিসন ):
- [RO-P (O) 2 -OPO (O) 2 -O-PO 3 ] 4− + H
2O
H
2O → [RO-P (O) 2 -O-PO 3 ] 3− + [পিও 4 ] 3− + 2 H + - [আরও-পি (ও) 2 -ওপিও (ও) 2 -ও-পিও 3 ] 4− + H
2O </br> H
2O → [আরও-পোও 3 ] 2− + [হে 3 পিও-পিও 3 ] 4− + 2 এইচ +
তথ্যসূত্র
সম্পাদনা- ↑ ক খ "Adenosine 5'-triphosphate disodium salt Product Information" (পিডিএফ)। Sigma। ২০১৯-০৩-২৩ তারিখে মূল (পিডিএফ) থেকে আর্কাইভ করা। সংগ্রহের তারিখ ২০১৯-০৩-২২।
- ↑ জীববিজ্ঞান - জীবনি শক্তি - নবম - দশম শ্রেনী (মাধ্যমিক বিদ্যালয়)। শিক্ষাবোর্ড বাংলাদেশ। ২০১৭। পৃষ্ঠা ৬৬,৬৭।
- ↑ Knowles, J. R. (১৯৮০)। "Enzyme-catalyzed phosphoryl transfer reactions": 877–919। ডিওআই:10.1146/annurev.bi.49.070180.004305। পিএমআইডি 6250450।
- ↑ Törnroth-Horsefield, S.; Neutze, R. (ডিসেম্বর ২০০৮)। "Opening and closing the metabolite gate": 19565–19566। ডিওআই:10.1073/pnas.0810654106। পিএমআইডি 19073922। পিএমসি 2604989 ।
- ↑ ক খ Storer, A.; Cornish-Bowden, A. (১৯৭৬)। "Concentration of MgATP2− and other ions in solution. Calculation of the true concentrations of species present in mixtures of associating ions": 1–5। ডিওআই:10.1042/bj1590001। পিএমআইডি 11772। পিএমসি 1164030 ।
- ↑ Wilson, J.; Chin, A. (১৯৯১)। "Chelation of divalent cations by ATP, studied by titration calorimetry": 16–19। ডিওআই:10.1016/0003-2697(91)90036-S। পিএমআইডি 1645933।
- ↑ Garfinkel, L.; Altschuld, R. (১৯৮৬)। "Magnesium in cardiac energy metabolism": 1003–1013। ডিওআই:10.1016/S0022-2828(86)80289-9। পিএমআইডি 3537318।
- ↑ Saylor, P.; Wang, C. (১৯৯৮)। "A second magnesium ion is critical for ATP binding in the kinase domain of the oncoprotein v-Fps": 12624–12630। ডিওআই:10.1021/bi9812672। পিএমআইডি 9730835।
- ↑ Lin, X.; Ayrapetov, M (২০০৫)। "Characterization of the interactions between the active site of a protein tyrosine kinase and a divalent metal activator": 25। ডিওআই:10.1186/1471-2091-6-25। পিএমআইডি 16305747। পিএমসি 1316873 ।
- ↑ Ferguson, S. J.; Nicholls, David (২০০২)। Bioenergetics 3 (3rd সংস্করণ)। Academic। আইএসবিএন 978-0-12-518121-1।
- ↑ Berg, J. M.; Tymoczko, J. L. (২০০৩)। Biochemistry। W. H. Freeman। পৃষ্ঠা 376। আইএসবিএন 978-0-7167-4684-3।
- ↑ Chance, B.; Lees, H. (১৯৭২)। "The Meaning of "Reversed Electron Flow" and "High Energy Electron" in Biochemistry": 330–331। ডিওআই:10.1038/238330a0। পিএমআইডি 4561837।
- ↑ Gajewski, E.; Steckler, D. (১৯৮৬)। "Thermodynamics of the hydrolysis of adenosine 5′-triphosphate to adenosine 5′-diphosphate" (পিডিএফ): 12733–12737। পিএমআইডি 3528161। ২০০৭-০৯-২৭ তারিখে মূল (পিডিএফ) থেকে আর্কাইভ করা। সংগ্রহের তারিখ ২০০৬-১২-২৭।
- ↑ Berg, Jeremy M.; Tymoczko, John L. (২০০৭)। Biochemistry (6th সংস্করণ)। W. H. Freeman। পৃষ্ঠা 413। আইএসবিএন 978-0-7167-8724-2।