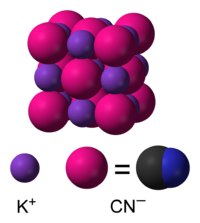
পটাসিয়াম সায়ানাইড
পটাশিয়াম সায়ানাইড হলো একটি যৌগ যার রাসায়নিক সংকেত KCN। চিনির মতো দেখতে এই বর্ণহীন স্ফটিক লবণটি জলে অত্যন্ত দ্রবণীয়। বেশিরভাগ পটাশিয়াম সায়ানাইড খনি থেকে স্বর্ণ উত্তোলনে, জৈব সংশ্লেষণ এবং ইলেক্ট্রোপ্লেটিংয়ে ব্যবহার করা হয়। অলঙ্কারশিল্পে রাসায়নিক গিল্ডিংয়ে (সোনার প্রলেপ দেওয়া) ও পালিশিংয়ে এর অল্প পরিসরে প্রয়োগ রয়েছে।[৪]
| |

| |
| নামসমূহ | |
|---|---|
| ইউপ্যাক নাম
Potassium cyanide
| |
| শনাক্তকারী | |
ত্রিমাত্রিক মডেল (জেমল)
|
|
| সিএইচইবিআই | |
| কেমস্পাইডার | |
| ইসিএইচএ ইনফোকার্ড | ১০০.০০৫.২৬৭ |
| ইসি-নম্বর |
|
পাবকেম CID
|
|
| আরটিইসিএস নম্বর |
|
| ইউএনআইআই | |
| ইউএন নম্বর | 1680 |
কম্পটক্স ড্যাশবোর্ড (EPA)
|
|
| |
| |
| বৈশিষ্ট্য | |
| KCN | |
| আণবিক ভর | 65.12 g/mol |
| বর্ণ | White crystalline solid deliquescent |
| গন্ধ | faint, almond-like |
| ঘনত্ব | 1.52 g/cm3 |
| গলনাঙ্ক | ৬৩৪.৫ °সে (১,১৭৪.১ °ফা; ৯০৭.৬ K) |
| স্ফুটনাঙ্ক | ১,৬২৫ °সে (২,৯৫৭ °ফা; ১,৮৯৮ K) |
| 71.6 g/100 ml (25 °C) 100 g/100 mL (100 °C) | |
| দ্রাব্যতা in methanol | 4.91 g/100 mL (20 °C) |
| দ্রাব্যতা in glycerol | soluble |
| দ্রাব্যতা in formamide | 14.6 g/100 mL |
| দ্রাব্যতা in ethanol | 0.57 g/100mL |
| দ্রাব্যতা in hydroxylamine | 41 g/100 mL |
| অম্লতা (pKa) | 11.0 |
| −37.0·10−6 cm3/mol | |
| প্রতিসরাঙ্ক (nD) | 1.410 |
| তাপ রসায়নবিদ্যা | |
| স্ট্যন্ডার্ড মোলার এন্ট্রোফি এস |
127.8 J K−1 mol−1 |
| গঠনে প্রমান এনথ্যাল্পির পরিবর্তন ΔfH |
−131.5 kJ/mol |
| ঝুঁকি প্রবণতা | |
| নিরাপত্তা তথ্য শীট | ICSC 0671 |
| জিএইচএস চিত্রলিপি |    
|
| জিএইচএস সাংকেতিক শব্দ | বিপদজনক |
| জিএইচএস বিপত্তি বিবৃতি | H290, H300, H310, H330, H370, H372, H410 |
| জিএইচএস সতর্কতামূলক বিবৃতি | P260, P264, P273, P280, P284, P301+310 |
| এনএফপিএ ৭০৪ | |
| ফ্ল্যাশ পয়েন্ট | Non-flammable |
| প্রাণঘাতী ডোজ বা একাগ্রতা (LD, LC): | |
LD৫০ (মধ্যমা ডোজ)
|
5 mg/kg (oral, rabbit) 10 mg/kg (oral, rat) 5 mg/kg (oral, rat) 8.5 mg/kg (oral, mouse)[২] |
| যুক্তরাষ্ট্রের স্বাস্থ্য অনাবৃতকরণ সীমা (NIOSH): | |
PEL (অনুমোদনযোগ্য)
|
TWA 5 mg/m3[১] |
REL (সুপারিশকৃত)
|
C 5 mg/m3 (4.7 ppm) [10-minute][১] |
IDLH (তাৎক্ষণিক বিপদ
|
25 mg/m3[১] |
| সম্পর্কিত যৌগ | |
অন্যান্য অ্যানায়নসমূহ
|
Potassium cyanate Potassium thiocyanate |
অন্যান্য ক্যাটায়নসমূহ
|
Sodium cyanide Rubidium cyanide lithium cyanide caesium cyanide |
সম্পর্কিত যৌগ
|
Hydrogen cyanide |
সুনির্দিষ্টভাবে উল্লেখ করা ছাড়া, পদার্থসমূহের সকল তথ্য-উপাত্তসমূহ তাদের প্রমাণ অবস্থা (২৫ °সে (৭৭ °ফা), ১০০ kPa) অনুসারে দেওয়া হয়েছে। | |
| তথ্যছক তথ্যসূত্র | |
পটাশিয়াম সায়ানাইড অত্যন্ত বিষাক্ত। আর্দ্র কঠিন পটাশিয়াম সায়ানাইডের আর্দ্র বিশ্লেষণের ফলে এটা থেকে অল্প পরিমাণে হাইড্রোজেন সায়ানাইড নির্গত হয়, যার গন্ধ তেতো বাদামের মতো।[৫] যাইহোক, সবাই এই গন্ধ শুঁকতে পারে না; যাদের এই ক্ষমতা রয়েছে তাদের এই ক্ষমতাটি একটি বংশাণুক্রমিক বৈশিষ্ট্য।[৬]
পটাশিয়াম সায়ানাইডের স্বাদকে তীক্ষ্ণ এবং তিক্ত হিসেবে বর্ণনা করা হয়েছে, এটি লাইয়ের (এপলক প্রকার ক্ষার) মতো জ্বলন্ত সংবেদন তৈরি করে।[৭] । [৮]
উৎপাদন সম্পাদনা
পটাশিয়াম হাইড্রোক্সাইডের জলীয় দ্রবণের সাথে হাইড্রোজেন সায়ানাইড যোগ করে শূন্যস্থানে দ্রআণটির বাষ্পীভবন থেকে KCN উউপাদন করা হয়।:[৯]
প্রতিবছর প্রায় ৫০ হাজার টন পটাশিয়াম সায়ানাইড উৎপাদন করা হয়।[৪]
পুরনো পদ্ধতিতে উৎপাদন সম্পাদনা
১৯০০ সালের আগে এবং কাস্টনার পদ্ধতি আবিষ্কারের পূর্বে পটাশিয়াম সায়ানাইড ছিল ক্ষার ধাতুর সায়ানাইডের সবচেয়ে গুরুত্বপূর্ণ উৎস।[৪] প্রাচীন এই পদ্ধতিতে পটাশিয়াম ফেরোসায়ানাইডের ভাঙ্গন থেকে পটাশিয়াম সায়ানাইড উৎপাদন করা হতো।:[১০]
তথ্যসূত্র সম্পাদনা
- ↑ ক খ গ "NIOSH Pocket Guide to Chemical Hazards #0522" (ইংরেজি ভাষায়)। ন্যাশনাল ইনস্টিটিউট ফর অকুপেশনাল সেফটি অ্যান্ড হেলথ (NIOSH)।
- ↑ "Cyanides (as CN)"। স্বাস্থ্য এবং জীবনের জন্য সহসা ঝুঁকিপূর্ণ। National Institute for Occupational Safety and Health (NIOSH)।
- ↑ "POTASSIUM CYANIDE | CAMEO Chemicals | NOAA"।
- ↑ ক খ গ Andreas Rubo, Raf Kellens, Jay Reddy, Joshua Wooten, Wolfgang Hasenpusch "Alkali Metal Cyanides" in Ullmann's Encyclopedia of Industrial Chemistry 2006 Wiley-VCH, Weinheim, Germany. ডিওআই:10.1002/14356007.i01_i01
- ↑ "Suicide note reveals taste of cyanide"। ২০০৬-০৭-০৮।
- ↑ অনলাইন মেন্ডেলিয়ান ইনহেরিটেন্স ইন ম্যান (ওএমআইএম): ৩০৪৩০০
- ↑ ലേഖകൻ, മാധ്യമം (২০২১-১২-১৯)। "'സയനൈഡ് ചവർപ്പാണ്... പുകച്ചിലാണ്...'; ആ 'രുചി രഹസ്യം' പുറത്തുവിട്ട മലയാളി നടന്ന വഴിയിലൂടെ | Madhyamam"। www.madhyamam.com (মালায়ালাম ভাষায়)। সংগ্রহের তারিখ ২০২১-১২-২১।
- ↑ "The only taste: Cyanide is acrid"। hindustantimes.com। Hindustan Times। ২০০৬-০৭-০৮।
- ↑ Pradyot Patnaik. Handbook of Inorganic Chemicals. McGraw-Hill, 2002, আইএসবিএন ০-০৭-০৪৯৪৩৯-৮
- ↑ Von Wagner, Rudolf (১৮৯৭)। Manual of chemical technology। New York: D. Appleton & Co.। পৃষ্ঠা 474 & 477।
