গুটিবসন্ত টিকা
নিম্নলিখিত নিবন্ধটির বর্তমানে "অন্য ভাষা" থেকে বাংলায় অনুবাদের কাজ চলছে। দয়া করে এটি অনুবাদ করে আমাদেরকে সহায়তা করুন। যদি অনুবাদ করা শেষ হয়ে থাকে তাহলে এই নোটিশটি সরিয়ে নিন। |
গুটিবসন্তের টিকা ছিল একটি সংক্রামক রোগের বিরুদ্ধে তৈরি করা প্রথম টিকা। ১৭৯৬ সালে ব্রিটিশ ডাক্তার এডওয়ার্ড জেনার দেখিয়েছিলেন যে তুলনামূলকভাবে হালকা গো-বসন্ত ভাইরাসের সংক্রমণ মারাত্মক গুটিবসন্ত ভাইরাসের বিরুদ্ধে অনাক্রম্যতা প্রদান করে। বিংশ শতকে আধুনিক গুটিবসন্ত ভ্যাকসিন আবির্ভূত হওয়া পর্যন্ত গরুবসন্ত একটি প্রাকৃতিক ভ্যাকসিন হিসাবে কাজ করেছিল। ১৯৫৮ থেকে ১৯৭৭ সাল পর্যন্ত, বিশ্ব স্বাস্থ্য সংস্থা একটি বিশ্বব্যাপী টিকাদান অভিযান পরিচালনা করেছিল যা গুটিবসন্ত নির্মূল করেছিল, এটিকে একমাত্র মানবজাতির রোগ থেকে নির্মূল করার জন্য। যদিও বাঁধা-ধরাভাবে গুটিবসন্তের টিকা সাধারণ জনগণের উপর আর সঞ্চালিত হয় না, তবুও জৈবসন্ত্রাস, জৈবিক যুদ্ধবিগ্রহ এবং মাংকিপক্স থেকে রক্ষা করার জন্য এখনও ভ্যাকসিন তৈরি করা হচ্ছে।[২][৩]
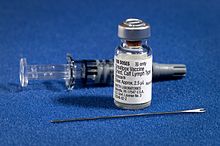 ড্রাইভ্যাক্স শুকনো গুটিবসন্ত ভ্যাকসিন এবং দ্বিখণ্ডিত সুইয়ের শিশির পাশাপাশি একটি সিরিঞ্জে মিশ্রিত গুটিবসন্তের টিকা | |
| টিকার বিবরণ | |
|---|---|
| লক্ষ্য ব্যাধি | গুটিবসন্ত |
| প্রকার | জীবন্ত ভাইরাস |
| রোগশয্যাসম্বন্ধীয় তথ্য | |
| বাণিজ্যিক নাম | ACAM2000, Imvanex, Jynneos, others |
| এএইচএফএস/ ড্রাগস.কম | / ভুক্তি |
| লাইসেন্স উপাত্ত | |
| গর্ভাবস্থার শ্রেণি | |
| প্রয়োগের স্থান | Subcutaneous injection |
| এটিসি কোড |
|
| আইনি অবস্থা | |
| আইনি অবস্থা | |
| শনাক্তকারী | |
| ড্রাগব্যাংক | |
| ইউএনআইআই | |
টিকা অর্থাৎ ভ্যাকসিন শব্দটি গরুর অর্থে ল্যাটিন শব্দ থেকে এসেছে। যা গুটিবসন্তের টিকাদানের উৎপত্তিকে প্রতিফলিত করে। এডওয়ার্ড জেনার গো-বসন্তকে ভ্যারিওলা ভ্যাকসিন (গরুর গুটিবসন্ত) বলে উল্লেখ করেছেন। গুটি বসন্তের ভ্যাকসিনের উৎপত্তি সময়ের সাথে সাথে অস্পষ্ট হয়ে ওঠে[৪] বিশেষ করে ১৯ শতকে লুই পাস্তুর যখন ভ্যাকসিন তৈরির জন্য ল্যাবরেটরি তৈরি করার কৌশল ব্যবহার করেন। ১৯৩৯ সালে অ্যালান ওয়াট ডাউনি দেখিয়েছিলেন যে আধুনিক গুটি বসন্তের ভ্যাকসিন সেরোলজিক্যাল ভাবে গো-বসন্ত থেকে আলাদা[৫]এবং ভ্যাক্সিনিয়া পরবর্তীকালে একটি পৃথক ভাইরাস প্রজাতি হিসেবে স্বীকৃত হয়। সম্পূর্ণ-জিনোম সিকোয়েন্সিং প্রকাশ করেছে যে ভ্যাক্সিনিয়া ঘোড়ার পক্সের সাথে সবচেয়ে ঘনিষ্ঠভাবে সম্পর্কিত, এবং গ্রেট ব্রিটেনে পাওয়া কাউপক্স স্ট্রেনগুলি টিকার সাথে সবচেয়ে কম ঘনিষ্ঠভাবে সম্পর্কিত।[৬]
প্রকারভেদ
সম্পাদনাবাছুরের লিম্ফ
সম্পাদনাউনিশ শতকে ব্যবহৃত গুটিবসন্তের ভ্যাকসিনের একটি[৭] নাম ছিল বাছুরের লিম্ফ এবং যা ১৯৭০ সাল থেকে এখনও পর্যন্ত তৈরি করা হয়েছিল। বাছুরের লিম্ফ রোগটি ১৮০৫ সালের প্রথম দিকে ইতালিতে পরিচিত ছিল[৮] কিন্তু এটি ছিল ১৮৬৪ সালের লিয়ন মেডিকেল সম্মেলন যা কৌশলটিকে বিস্তৃত বিশ্বের কাছে পরিচিত করে তোলে।[৯] ১৮৯৮ সালে বাছুরের লিম্ফ যুক্তরাজ্যে গুটিবসন্তের জন্য টিকা দেওয়ার আদর্শ পদ্ধতি হয়ে ওঠে, তখন বাহু থেকে বাহুতে টিকা দেওয়া শেষ পর্যন্ত নিষিদ্ধ করা হয়েছিল[১০][১১] (সিফিলিস, ইরিসিপেলাস বা গুটিবসন্তের একযোগে সংক্রমণের মতো জটিলতার কারণে)[১২]
ড্রাইভ্যাক্স
সম্পাদনাDryvax was a freeze-dried live-virus smallpox vaccine prepared from calf lymph and used for smallpox eradication efforts.[১৪] The vaccine was effective, providing successful immunogenicity in about 95% of vaccinated persons. Dryvax has serious adverse side-effects in about 1% to 2% of cases.[১৫]
Before its discontinuation, it was the world's oldest smallpox vaccine, created in the late 19th century by American Home Products, a predecessor of Wyeth. It was developed from the New York City Board of Health (NYCBOH) strain.[১৬] By the 1940s, Wyeth was the leading U.S. manufacturer of the vaccine and the only manufacturer by the 1960s. After world health authorities declared smallpox had been eradicated from nature in 1980, Wyeth stopped making the vaccine.[১৭] The U.S. Centers for Disease Control and Prevention (CDC) kept a stockpile for use in case of emergency. In 2003 this supply helped contain an outbreak of monkeypox in the United States.[৩] In February 2008, the CDC disposed of the last of its 12 million doses of Dryvax. Its supply was replaced by ACAM2000,[১৮] a more modern product manufactured in laboratories by Acambis, a division of Sanofi Pasteur.[১৭][১৯][২০]
Trace amounts of the following antibiotics (added during processing) may have been present in Dryvax: neomycin sulfate, chlortetracycline hydrochloride, polymyxin B sulfate, and dihydrostreptomycin sulfate.[২১]
ACAM2000
সম্পাদনাACAM2000 is a smallpox vaccine developed by Acambis. It was approved for use in the United States by the Food and Drug Administration (FDA) on 31 August 2007.[১৮] It contains live vaccinia virus, cloned from the same strain used in an earlier vaccine, Dryvax. While the Dryvax virus was cultured in the skin of calves and freeze-dried, ACAM2000s virus is cultured in kidney epithelial cells (Vero cells) from an African green monkey. Efficacy and adverse reaction incidence are similar to Dryvax.[১৫] The vaccine is not routinely available to the U.S. public; it is, however, used in the military and maintained in the Strategic National Stockpile.[১৪][২২]
A droplet of ACAM2000 is administered by the percutaneous route (scarification) using 15 jabs of a bifurcated needle. ACAM2000 should not be injected by the intradermal, subcutaneous, intramuscular, or intravenous route.[২৩]
এমভিএ-বিএন
সম্পাদনা
| টিকার বিবরণ | |
|---|---|
| লক্ষ্য ব্যাধি | গুটিবসন্ত |
| প্রকার | ক্ষুদ্র টিকা |
| রোগশয্যাসম্বন্ধীয় তথ্য | |
| বাণিজ্যিক নাম | ইমভানেক্স, ইমভামুন, জিনিওস |
| এএইচএফএস/ ড্রাগস.কম | |
| প্রয়োগের স্থান | সাবকিউটেনিয়াস ইনজেকশন |
| এটিসি কোড | |
| আইনি অবস্থা | |
| আইনি অবস্থা | |
| শনাক্তকারী | |
| কেমস্পাইডার |
|
MVA-BN (also known as: Imvanex in the European Union; Imvamune in Canada; and Jynneos[১৪][২৫] in the United States) is a live, non-replicating vaccine for smallpox and monkeypox developed and manufactured by Bavarian Nordic and derived from Modified Vaccinia Ankara, an attenuated strain of the vaccinia virus. It was approved in the European Union for immunization against smallpox disease in adults in July 2013,[২৪] and was approved in Canada.[২৬][২৭][২৮] MVA-BN underwent further clinical trials in preparation for approval in the United States,[২৯][৩০][৩১] and was approved by the U.S. Food and Drug Administration (FDA) in September 2019.[৩২][৩৩]
MVA-BN contains Modified vaccinia Ankara, an attenuated form of the vaccinia virus that does not replicate in human cells and hence does not cause the sometimes serious side effects that are seen with replicating smallpox vaccines (i.e. preparations of unattenuated vaccinia virus). These replicating vaccines use different strains of the vaccinia virus, which all replicate in humans, and are not recommended for people with immune deficiencies and exfoliative skin disorders, such as eczema or atopic dermatitis. Vaccines containing vaccinia viruses were used effectively in the campaign to eradicate smallpox. Because of similarities between vaccinia and the smallpox virus, the antibodies produced against vaccinia have been shown to protect against smallpox. In contrast to replicating smallpox vaccines, which are applied by scarification using a bifurcated needle, MVA-BN is administered by injection via the subcutaneous route.[৩৪]
আগস্ট ২০১৪-এর হিসাব অনুযায়ী[হালনাগাদ], 24 million doses of MVA-BN were delivered to the U.S. Strategic National Stockpile (SNS) for use by people with weakened immune systems or atopic dermatitis.[১৪]
তথ্যসূত্র
সম্পাদনা- ↑ "Smallpox vaccine Use During Pregnancy"। Drugs.com। ৩ জানুয়ারি ২০২০। সংগ্রহের তারিখ ২২ জানুয়ারি ২০২০।
- ↑ Metzger W, Mordmueller BG, ও অন্যান্য (The Cochrane Collaboration) (জুলাই ২০০৭)। Metzger W, সম্পাদক। "Vaccines for preventing smallpox"। The Cochrane Database of Systematic Reviews। Chichester, UK: John Wiley & Sons, Ltd (3): CD004913। ডিওআই:10.1002/14651858.cd004913। পিএমআইডি 17636779। পিএমসি 6532594 ।
- ↑ ক খ Anderson MG, Frenkel LD, Homann S, and Guffey J. (2003), "A case of severe monkeypox virus disease in an American child: emerging infections and changing professional values"; Pediatr Infect Dis J;22(12): 1093–96; discussion 1096–98.
- ↑ Baxby D (১৯৮১)। Jenner's Smallpox Vaccine: The Riddle of Vaccinia Virus and Its Origin (ইংরেজি ভাষায়)। Heinemann Educational Books। আইএসবিএন 978-0-435-54057-9।
- ↑ উদ্ধৃতি ত্রুটি:
<ref>ট্যাগ বৈধ নয়;downie1939নামের সূত্রটির জন্য কোন লেখা প্রদান করা হয়নি - ↑ Carroll DS, Emerson GL, Li Y, Sammons S, Olson V, Frace M, ও অন্যান্য (৮ আগস্ট ২০১১)। "Chasing Jenner's vaccine: revisiting cowpox virus classification"। PLOS ONE। 6 (8): e23086। ডিওআই:10.1371/journal.pone.0023086 । পিএমআইডি 21858000। পিএমসি 3152555 । বিবকোড:2011PLoSO...623086C।
- ↑ BMA (১৯০৫)। Facts about Smallpox and Vaccination। British Medical Association। পৃষ্ঠা 21। সংগ্রহের তারিখ ৭ জানুয়ারি ২০২১।
- ↑ Galbiati G (১৮১০)। Memoria Sulla Inoculazione Vaccina coll'Umore Ricavato Immediatement dalla Vacca Precedentemente Inoculata। Napoli।
- ↑ Congrès Medical de Lyon (১৮৬৪)। "Compterendu des travaux et des discussions"। Gazette Med Lyon। 19: 449–71।
- ↑ Brown E (১৯০২)। The Case for vaccination। Baillière, Tindall & Cox। পৃষ্ঠা 8, 21।
- ↑ Ballard E (১৮৬৮)। On Vaccination: Its Value and Alleged Dangers। London।
- ↑
Didgeon JA (মে ১৯৬৩)। "Development of Smallpox Vaccine in England in the Eighteenth and Nineteenth Centuries"। British Medical Journal। 1 (5342): 1367–72। ডিওআই:10.1136/bmj.1.5342.1367। পিএমআইডি 20789814। পিএমসি 2124036 । - ↑ Rubin BA (মে ১৯৮০)। "A note on the development of the bifurcated needle for smallpox vaccination"। WHO Chronicle। 34 (5): 180–81। পিএমআইডি 7376638।
- ↑ ক খ গ ঘ "Smallpox Vaccine Supply & Strength"। National Institute of Allergy and Infectious Diseases (NIAID)। ২৬ সেপ্টেম্বর ২০১৯। ১৭ অক্টোবর ২০১৯ তারিখে মূল থেকে আর্কাইভ করা। সংগ্রহের তারিখ ১৬ অক্টোবর ২০১৯।
- ↑ ক খ Metzger W, Mordmueller BG (জুলাই ২০০৭)। "Vaccines for preventing smallpox"। The Cochrane Database of Systematic Reviews (3): CD004913। ডিওআই:10.1002/14651858.CD004913.pub2। পিএমআইডি 17636779। পিএমসি 6532594 ।
- ↑ Davies, D. Huw; ও অন্যান্য (১৫ জানুয়ারি ২০০৮)। "Antibody Profiling by Proteome Microarray Reveals the Immunogenicity of the Attenuated Smallpox Vaccine Modified Vaccinia Virus Ankara Is Comparable to That of Dryvax"। Journal of Virology। 82 (2): 652–663। ডিওআই:10.1128/JVI.01706-07। পিএমআইডি 17977963। ২১ মে ২০২২ তারিখে মূল থেকে আর্কাইভ করা। সংগ্রহের তারিখ ২১ মে ২০২২।
- ↑ ক খ "CDC to Destroy Oldest Smallpox Vaccine"। Associated Press। ৩ মার্চ ২০০৮। সংগ্রহের তারিখ ২০১৯-০৮-২৬।
- ↑ ক খ "ACAM2000"। U.S. Food and Drug Administration (FDA)। ২০১৮-০৯-২০। STN BL 125158। ১৭ অক্টোবর ২০১৯ তারিখে মূল থেকে আর্কাইভ করা। সংগ্রহের তারিখ ১৬ অক্টোবর ২০১৯।
- ↑ "Safety Surveillance Study of ACAM2000 Vaccinia Vaccine"। clinicaltrials.gov। ২৯ জানুয়ারি ২০১৯। সংগ্রহের তারিখ ১৬ অক্টোবর ২০১৯।
- ↑ Roos, Robert (৭ মার্চ ২০০৮)। "CDC retires one old smallpox vaccine, keeps another"। CIDRAP - Center for Infectious Disease Research and Policy। সংগ্রহের তারিখ ২১ মে ২০২২।
- ↑ Wyeth package insert / U.S. Food and Drug Administration
- ↑ FDA/CBER Questions and Answers; Medication Guide; accessed 1 March 2008.
- ↑ Emergent Product Development Gaithersburg Inc.। "Highlights of Prescribing Information: ACAM2000, (Smallpox (Vaccinia) Vaccine, Live)" (পিডিএফ)। U.S. Food and Drug Administration। এই উৎস থেকে এই নিবন্ধে লেখা অন্তর্ভুক্ত করা হয়েছে, যা পাবলিক ডোমেইনে রয়েছে।
- ↑ ক খ "Imvanex EPAR"। European Medicines Agency (EMA)। সংগ্রহের তারিখ ২০১৪-১০-০২।
- ↑ Greenberg RN, Hay CM, Stapleton JT, Marbury TC, Wagner E, Kreitmeir E, ও অন্যান্য (২০১৬)। "A Randomized, Double-Blind, Placebo-Controlled Phase II Trial Investigating the Safety and Immunogenicity of Modified Vaccinia Ankara Smallpox Vaccine (MVA-BN®) in 56–80-Year-Old Subjects"। PLOS ONE। 11 (6): e0157335। ডিওআই:10.1371/journal.pone.0157335 । পিএমআইডি 27327616। পিএমসি 4915701 । বিবকোড:2016PLoSO..1157335G।
- ↑ "Smallpox vaccine: Canadian Immunization Guide"। Public Health Agency of Canada। জানুয়ারি ২০১৪। সংগ্রহের তারিখ ২৪ জুন ২০২০।
- ↑ "Register of Innovative Drugs" (পিডিএফ)। Health Canada। জুন ২০২০। ২৬ জুন ২০২০ তারিখে মূল (পিডিএফ) থেকে আর্কাইভ করা। সংগ্রহের তারিখ ২৪ জুন ২০২০। lay summary।
- ↑ "Products for Human Use. Submission #144762"। Register of Innovative Drugs। Health Canada। ২০১৪-০৬-১৭ তারিখে মূল থেকে আর্কাইভ করা। সংগ্রহের তারিখ ২০১৪-১০-৩০।
- ↑ "Infectious Diseases: Clinical Trials"। Bavarian Nordic। ২৬ এপ্রিল ২০১৬ তারিখে মূল থেকে আর্কাইভ করা। সংগ্রহের তারিখ ২০১৪-১০-৩০।
- ↑ "Phase II Trial to Assess Safety and Immunogenicity of Imvamune"। ClinicalTrials.gov। U.S. National Institutes of Health। সংগ্রহের তারিখ ২০১৪-১০-৩০।
- ↑ Pittman PR, Hahn M, Lee HS, Koca C, Samy N, Schmidt D, ও অন্যান্য (নভেম্বর ২০১৯)। "Phase 3 Efficacy Trial of Modified Vaccinia Ankara as a Vaccine against Smallpox"। The New England Journal of Medicine। 381 (20): 1897–1908। ডিওআই:10.1056/NEJMoa1817307 । পিএমআইডি 31722150।
- ↑ "Jynneos"। U.S. Food and Drug Administration (FDA)। ২৪ সেপ্টেম্বর ২০১৯। STN 125678। ১৭ অক্টোবর ২০১৯ তারিখে মূল থেকে আর্কাইভ করা। সংগ্রহের তারিখ ১৬ অক্টোবর ২০১৯। এই উৎস থেকে এই নিবন্ধে লেখা অন্তর্ভুক্ত করা হয়েছে, যা পাবলিক ডোমেইনে রয়েছে।
- ↑ "FDA approves first live, non-replicating vaccine to prevent smallpox and monkeypox"। U.S. Food and Drug Administration (FDA)। ২৪ সেপ্টেম্বর ২০১৯। ১৭ অক্টোবর ২০১৯ তারিখে মূল থেকে আর্কাইভ করা। সংগ্রহের তারিখ ১৭ অক্টোবর ২০১৯। এই উৎস থেকে এই নিবন্ধে লেখা অন্তর্ভুক্ত করা হয়েছে, যা পাবলিক ডোমেইনে রয়েছে।
- ↑ "Summary Basis for Regulatory Action Template"। FDA। U.S. Food & Drug Administration। সংগ্রহের তারিখ ৮ অক্টোবর ২০২১।