কপার (I) ক্লোরাইড
কপার (I) ক্লোরাইড, সাধারণত কিউপ্রাস ক্লোরাইড নামে পরিচিত, যা কপারের একটি নিম্নতর ক্লোরাইড। এটির রাসায়নিক সংকেত CuCl। এটি সাদা কঠিন পদার্থ যা জলে প্রায় দ্রবণীয় নয় বললেই চলে, কিন্তু গাঢ় হাইড্রোক্লোরিক অ্যাসিডে অত্যন্ত দ্রবণীয়। কপার (II) ক্লোরাইড এর উপস্থিতির কারণে এর অবিশুদ্ধ নমুনাসমূহ সবুজ বর্ণের হয়। [৩]
| |

| |
| নামসমূহ | |
|---|---|
| ইউপ্যাক নাম
কপার(১) ক্লোরাইড
| |
| অন্যান্য নাম
কপার ক্লোরাইড
| |
| শনাক্তকারী | |
ত্রিমাত্রিক মডেল (জেমল)
|
|
| সিএইচইবিআই | |
| কেমস্পাইডার | |
| ইসিএইচএ ইনফোকার্ড | ১০০.০২৮.৯৪৮ |
| ইসি-নম্বর |
|
পাবকেম CID
|
|
| আরটিইসিএস নম্বর |
|
কম্পটক্স ড্যাশবোর্ড (EPA)
|
|
| |
| |
| বৈশিষ্ট্য | |
| CuCl | |
| আণবিক ভর | 98.999 g/mol |
| বর্ণ | white powder, slightly green from oxidized impurities |
| ঘনত্ব | 4.145 g/cm3 |
| গলনাঙ্ক | ৪২৬ °সে (৭৯৯ °ফা; ৬৯৯ K) |
| স্ফুটনাঙ্ক | ১,৪৯০ °সে (২,৭১০ °ফা; ১,৭৬০ K) (decomposes) |
| 0.0062 g/100 mL (20 °C) | |
Solubility product (Ksp)
|
1.72 x 10−7 |
| দ্রাব্যতা | insoluble in ethanol acetone; soluble in concentrated HCl, NH4OH |
| প্রতিসরাঙ্ক (nD) | 1.930[১] |
| গঠন | |
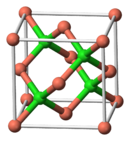
| স্ফটিক গঠন | Zinc blende structure |
| ঝুঁকি প্রবণতা | |
| নিরাপত্তা তথ্য শীট | JT Baker |
ইইউ শ্রেণীবিভাগ (ডিএসডি)
|
Harmful (Xn) Dangerous for the environment (N) |
| আর-বাক্যাংশ | আর২২, আর৫০/৫৩ |
| এস-বাক্যাংশ | (এস২), এস২২, এস৬০, এস৬১ |
| এনএফপিএ ৭০৪ | |
| ফ্ল্যাশ পয়েন্ট | Non-flammable |
| প্রাণঘাতী ডোজ বা একাগ্রতা (LD, LC): | |
LD৫০ (মধ্যমা ডোজ)
|
140 mg/kg |
| যুক্তরাষ্ট্রের স্বাস্থ্য অনাবৃতকরণ সীমা (NIOSH): | |
PEL (অনুমোদনযোগ্য)
|
TWA 1 mg/m3 (as Cu)[২] |
REL (সুপারিশকৃত)
|
TWA 1 mg/m3 (as Cu)[২] |
IDLH (তাৎক্ষণিক বিপদ
|
TWA 100 mg/m3 (as Cu)[২] |
| সম্পর্কিত যৌগ | |
অন্যান্য অ্যানায়নসমূহ
|
Copper(I) bromide Copper(I) iodide |
অন্যান্য ক্যাটায়নসমূহ
|
Copper(II) chloride Silver(I) chloride |
সুনির্দিষ্টভাবে উল্লেখ করা ছাড়া, পদার্থসমূহের সকল তথ্য-উপাত্তসমূহ তাদের প্রমাণ অবস্থা (২৫ °সে (৭৭ °ফা), ১০০ kPa) অনুসারে দেওয়া হয়েছে। | |
| তথ্যছক তথ্যসূত্র | |

ইতিহাস
সম্পাদনাসপ্তদশ শতাব্দীর মধ্যভাগে রবার্ট বয়েল কর্তৃক মারকিউরি(II) ক্লোরাইড ও কপার ধাতু হতে সর্বপ্রথম কপার (I) ক্লোরাইড প্রস্তুত হয়।[৪]:
- HgCl2 + 2Cu → 2CuCl + Hg
সংশ্লেষণ
সম্পাদনাতামা ধাতু এবং ক্লোরিনের সঙ্গে ৪৫০–৯০০ ডিগ্রি সেলসিয়াস তাপমাত্রায় সরাসরি বিক্রিয়া করে বাণিজ্যিকভাবে কপার (I) ক্লোরাইড তৈরি করা হয়।[৫][৬]
- 2 Cu + Cl2 -> 2 CuCl
সালফার ডাইঅক্সাইডের সাথে কপার(II) ক্লোরাইড হ্রাস করার মাধ্যমে কপার (I) ক্লোরাইড সংশ্লেষিত হয়:
2CuCl2 + SO2 + 2H2O → 2CuCl + H2SO4 + 2HCl
হ্রাস করার জন্য অন্যান্ন এজেন্ট ব্যবহার করা যেতে পারে[৭]।
রাসায়নিক বৈশিষ্ট্যাবলী
সম্পাদনা-
Copper(I) chloride
-
White copper(I) chloride crystals on copper wire
-
Copper(I) chloride partially oxidized in air
ব্যবহার
সম্পাদনাকপার (I) ক্লোরাইড এর মূল ব্যবহার হল ছত্রাকনাশক কপার অক্সিক্লোরাইড তৈরীতে। এই উদ্দেশ্যে জলীয় কপার (I) ক্লোরাইড কম্প্রোপোরশন্যাশন দ্বারা উতৎপন্ন করা হয় এবং এরপর বায়ুতে জারিত করা হয়:
- Cu + CuCl2 → 2CuCl
- 6CuCl + 3/2O2 + 3H2O → 2Cu3Cl2(OH)4 + CuCl2
জৈব সংশ্লেষণে
সম্পাদনাপলিমার রসায়নে
সম্পাদনাCuCl অনুঘটক হিসেবে এটম ট্রান্সফার র্যাডিক্যাল পলিমারাইজেসন (ATRP) এ ব্যবহৃত হয়।
তথ্যসূত্র
সম্পাদনা- ↑ Pradyot Patnaik. Handbook of Inorganic Chemicals. McGraw-Hill, 2002, আইএসবিএন ০-০৭-০৪৯৪৩৯-৮
- ↑ ক খ গ "NIOSH Pocket Guide to Chemical Hazards #0150" (ইংরেজি ভাষায়)। ন্যাশনাল ইনস্টিটিউট ফর অকুপেশনাল সেফটি অ্যান্ড হেলথ (NIOSH)।
- ↑ United States Patent US4582579 "method of preparing cupric ion free cuprous chloride" Section 2, lines 4-41 , via www.freepatentsonline.com
- ↑ Boyle, Robert (১৬৬৬)। Considerations and experiments about the origin of forms and qualities। Oxford। As reported in Mellor।
- ↑ Richardson, H. W. (২০০৩)। "Copper Compounds"। Kirk-Othmer Encyclopedia of Chemical Technology। আইএসবিএন 0471238961। ডিওআই:10.1002/0471238961.0315161618090308.a01.pub2।
- ↑ Zhang, J.; Richardson, H. W. (২০১৬)। "Copper Compounds"। Ullmann's Encyclopedia of Industrial Chemistry। পৃষ্ঠা 1–31। আইএসবিএন 978-3-527-30673-2। ডিওআই:10.1002/14356007.a07_567.pub2।
- ↑ O. Glemser and H. SauerR "Copper(I) Chloride" in Handbook of Preparative Inorganic Chemistry, 2nd Ed. Edited by G. Brauer, Academic Press, 1963, NY. Vol. 1. p. 1005.
আরও পড়ুন
সম্পাদনা- Mellor, J. W., A Comprehensive Treatise on Inorganic and Theoretical Chemistry, Volume III, pp157–168. Longmans, Green & Co., London, 1967 (new impression).
