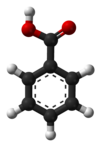
বেনজোয়িক অ্যাসিড: সংশোধিত সংস্করণের মধ্যে পার্থক্য
→ইতিহাস: পাতা তৈরি ট্যাগ: মোবাইল সম্পাদনা মোবাইল ওয়েব সম্পাদনা |
(কোনও পার্থক্য নেই)
|
১৪:০৬, ২৩ জুলাই ২০১৯ তারিখে সংশোধিত সংস্করণ
এই নিবন্ধটি ইংরেজি উইকিপিডিয়া হতে নিবন্ধ প্রতিযোগিতা ২০১৯ উপলক্ষে তৈরী করা হলো, নিবন্ধটিকে নির্দিষ্ট সময়ের মধ্যেই নিবন্ধকার কর্তৃক অনুবাদ দ্বারা মানোন্নয়ন ও সম্প্রসারণ করা হবে; আপনার যেকোন প্রয়োজনে এই নিবন্ধের আলাপ পাতাটি ব্যবহার করুন। আপনার আগ্রহের জন্য আপনাকে আন্তরিক ধন্যবাদ জানাচ্ছি। |
বেনজোয়িক আ্যসিড হল রংবিহীন স্বচ্ছ কঠিন এবং সরলতম আ্যরোমেটিক কার্বক্সিলিক আ্যসিড। নামটি আঠা জাতীয় পদার্থ বেনজোয়েন (রেজিন) থেকে করা হয়েছে, যেটি বহুসময় ধরে এটির একমাত্র জানা উৎস ছিল। বেনজোয়িক আ্যসিড প্রাকৃতিকভাবে বিভিন্ন গাছ থেকে উৎপন্ন হয় এবং অনেক দ্বিতীয় পর্যায়ের মেটাবোলাইটের জৈবসংশ্লেষনে অন্তর্বর্তী হিসাবে কাজ করে। বেনজোয়িক আ্যসিডের লবনগুলো খাদ্য সংরক্ষক হিসাবে ব্যবহার করা হয় এবং বেনজোয়িক আ্যসিড হল বিভিন্ন জৈব যৌগ প্রস্তুতির জন্য একটি গুরুত্বপূর্ণ যৌগ। বেনজোয়িক আ্যসিডের লবন ও এস্টারগুলো বেনজোয়েট নামে পরিচিত।
| |||

| |||
| নামসমূহ | |||
|---|---|---|---|
| পছন্দসই ইউপ্যাক নাম
বেনজোয়িক আ্যসিড (Benzoic acid)[১] | |||
| পদ্ধতিগত ইউপ্যাক নাম
বেনজিনকার্বক্সিলিক আ্যসিড | |||
অন্যান্য নাম
| |||
| শনাক্তকারী | |||
ত্রিমাত্রিক মডেল (জেমল)
|
|||
| থ্রিডিমেট | |||
| বেইলস্টেইন রেফারেন্স | ৬৩৬১৩১ | ||
| সিএইচইবিআই | |||
| সিএইচইএমবিএল | |||
| কেমস্পাইডার | |||
| ড্রাগব্যাংক | |||
| ইসিএইচএ ইনফোকার্ড | ১০০.০০০.৫৬২ | ||
| ইসি-নম্বর |
| ||
| ই নম্বর | E২১০ (সংরক্ষকদ্রব্য) | ||
| মেলিন রেফারেন্স | ২৯৪৬ | ||
| কেইজিজি | |||
| এমইএসএইচ | benzoic+acid | ||
পাবকেম CID
|
|||
| আরটিইসিএস নম্বর |
| ||
| ইউএনআইআই | |||
কম্পটক্স ড্যাশবোর্ড (EPA)
|
|||
| |||
| |||
| বৈশিষ্ট্য | |||
| C7H6O2 | |||
| আণবিক ভর | ১২২.১২ g·mol−১ | ||
| বর্ণ | রংবিহীন স্বচ্ছ কঠিন | ||
| গন্ধ | মৃদু | ||
| ঘনত্ব | ১.২৬৫৯ গ্রাম/সেমি৩ (১৫ °C) ১.০৭৪৯ গ্রাম/সেমি৩ (১৩০ °C)[২] | ||
| গলনাঙ্ক | ১২২ °সে (২৫২ °ফা; ৩৯৫ K)[৭] | ||
| স্ফুটনাঙ্ক | ২৫০ °সে (৪৮২ °ফা; ৫২৩ K)[৭] | ||
| ১.৭ গ্রাম/লিটার (০ °সে) ২.৭ গ্রাম/লিটার (১৮ °সে) ৩.৪৪ গ্রাম/লিটার (২৫ °সে) ৫.৫১ গ্রাম/লিটার (৪০ °সে) ২১.৪৫ গ্রাম/লিটার (৭৫ °সে) ৫৬.৩১ গ্রাম/লিটার (১০০ °সে)[২][৩] | |||
| দ্রাব্যতা | আ্যসিটোন, বেনজিন, CCl4, CHCl3, আ্যলকোহল, ইথাইল ইথার, হেক্সেন, ফিনাইল, তরল আ্যমোনিয়া, আ্যসিটেট এই দ্রাবকগুলোতে দ্রাব্য | ||
| লগ পি | ১.৮৭ | ||
| বাষ্প চাপ | ০.১৬ পাস্কাল (২৫ °সে) ০.১৯ কিলোপাস্কাল (১০০ °সে) ২২.৬ কিলোপাস্কাল (২০৯ °সে)[৪] | ||
| অম্লতা (pKa) | |||
| -৭০.২৮·১০−৬ সেমি৩/মোল | |||
| প্রতিসরাঙ্ক (nD) | ১.৫৩৯৭ (২০ °সে) ১.৫০৪ (১৩২ °সে)[২] | ||
| সান্দ্রতা | ১.২৬ মিলি পাস্কাল (১৩০ °সে) | ||
| গঠন | |||
| স্ফটিক গঠন | মনোক্লিনিক | ||
| আণবিক আকৃতি | সমতল | ||
| ডায়াপল মুহূর্ত | ১.৭২ ডিবাই ডাইঅক্সেনের মধ্যে | ||
| তাপ রসায়নবিদ্যা | |||
| তাপ ধারকত্ব, C | ১৪৬.৭ জুল/মোল·কেলভিন[৪] | ||
| স্ট্যন্ডার্ড মোলার এন্ট্রোফি এস |
১৬৭.৬ জুল/মোল·কেলভিন[২] | ||
| গঠনে প্রমান এনথ্যাল্পির পরিবর্তন ΔfH |
-৩৮৫.২ কিলোজুল/মোল[২] | ||
| দহনে প্রমান এনথ্যাল্পির পরিবর্তন ΔcH |
-৩২২৮ কিলোজুল/মোল[৪] | ||
| ঝুঁকি প্রবণতা | |||
| প্রধান ঝুঁকিসমূহ | যন্ত্রণাদায়ক | ||
| নিরাপত্তা তথ্য শীট | JT Baker | ||
| জিএইচএস চিত্রলিপি |   [৮] [৮]
| ||
| জিএইচএস সাংকেতিক শব্দ | বিপদজনক | ||
| জিএইচএস বিপত্তি বিবৃতি | H318, H335[৮] | ||
| জিএইচএস সতর্কতামূলক বিবৃতি | P261, P280, P305+351+338[৮] | ||
| এনএফপিএ ৭০৪ | |||
| ফ্ল্যাশ পয়েন্ট | ১২১.৫ °সে (২৫০.৭ °ফা; ৩৯৪.৬ K)[৭] | ||
| ৫৭১ °সে (১,০৬০ °ফা; ৮৪৪ K)[৭] | |||
| প্রাণঘাতী ডোজ বা একাগ্রতা (LD, LC): | |||
LD৫০ (মধ্যমা ডোজ)
|
1700 mg/kg (rat, oral) | ||
| সম্পর্কিত যৌগ | |||
সম্পর্কিত কার্বক্সিলিক আ্যসিড
|
হাইড্রক্সিবেনজয়িক আ্যসিড আ্যমিনোবেনজয়িক আ্যসিড, নাইট্রোবেনজয়িক আ্যসিড, ফিনাইলআ্যসিটিক আ্যসিড | ||
সম্পর্কিত যৌগ
|
বেঞ্জালডিহাইড, বেঞ্জাইল আ্যলকোহল, বেনজোইল ক্লোরাইড, বেঞ্জাইল আ্যমিন, বেঞ্জামাইড | ||
সুনির্দিষ্টভাবে উল্লেখ করা ছাড়া, পদার্থসমূহের সকল তথ্য-উপাত্তসমূহ তাদের প্রমাণ অবস্থা (২৫ °সে (৭৭ °ফা), ১০০ kPa) অনুসারে দেওয়া হয়েছে। | |||
| তথ্যছক তথ্যসূত্র | |||
ইতিহাস
ষোলোর দশকে বেনজোয়িক আ্যসিড আবিষ্কার হয়। আঠালো বেনজোয়েনের শুষ্ক পাতন প্রথম ব্যাখ্যা করেছিলেন নস্ট্রাদামুস (১৫৫৬ সাল), তারপর আলেক্সিউস পেডেমন্তনুস (১৫৬০) এবং ব্লাইসে দে ভিগেনরে (১৫৯৬)।
আমিগ্যালিনের উপর ভিত্তি করে ১৮৩০ সালের বিভিন্ন অভিজ্ঞতার কাজ, যা তিক্ত কাজুবাদামের তেল থেকে প্রাপ্ত দুই ফরাসি রসায়নবিদ দ্বারা, বেঞ্জালডিহাইড প্রস্তুত করেছিলেন। কিন্তু তারা আমিগ্যালিনের গঠনের সঠিক ব্যাখ্যার উপর কাজ করতে ব্যর্থ হয়েছিলেন, ফলে বেনজোইল র্যাডিকালের (C7H5O) উপস্থিতি তারা বুঝতে পারেননি। কয়েক মাস পরে জুউস ভন লিবিগ এবং ফ্রেডরিক ওয়ায়োলার ১৮৩২ সালে শেষ ধাপটি সম্পুর্ন করতে সক্ষম হন, যারা বেনজোয়িক আ্যসিডের কমপজিশন নির্ধারণ করেন। পরবর্তীতে আরও গবেষণা করে দেখা যায় যে হিপপিউরিক আ্যসিড কিভাবে বেনজোয়িক আ্যসিডের সাথে সম্পর্কিত ।
১৮৭৫ সালে সালকউস্কি (একজন বিজ্ঞানী) বেনজোয়িক আ্যসিডের অ্যান্টিফাঙ্গাল ক্ষমতা আবিষ্কার করেন, যা দীর্ঘদিন ধরে ব্যবহার করা হত বেনজোয়েট-যুক্ত ক্লাউডবেরি ফল সংরক্ষণে ।
এটি একটি রাসায়নিক যৌগ যা ক্যাস্টোরমে পাওয়া যায়। উত্তর আমেরিকার বিভার ক্যাস্টর থলি থেকে এই যৌগ জড়ো করা হয়।
উৎপাদন
শিল্পে প্রস্তুতি
বেনজোয়িক আ্যসিড অক্সিজেনের সাথে টলুইনের আংশিক জারণের (অক্সিডেশন) দ্বারা বাণিজ্যিকভাবে উৎপাদিত করা হয়। বিক্রিয়াটি কোবাল্ট বা ম্যাঙ্গানিজ ন্যাপথেনেট দ্বারা ত্বরান্বিত করা হয়। বিক্রিয়াটিতে প্রচুর উপকরণ ব্যবহৃৎ হয়, উচ্চ ফলাফলের সাথে এগিয়ে যায়।
শিল্পে প্রথম পদ্ধতিটি ছিল বেনজোট্রাইক্লোরাইডের (ট্রাইক্লোরোমিথাইল বেনজিন) সাথে ক্যালসিয়াম হাইড্রোঅক্সাইডের জলের মধ্যে বিক্রিয়া, আয়রন (লোহা) বা আয়রন সল্ট অনুঘটক হিসাবে ব্যবহার করে। প্রাপ্ত ক্যালসিয়াম বেনজোয়েটকে হাইড্রোক্লোরিক আ্যসিড দিয়ে বেনজোয়িক আ্যসিডে রূপান্তরিত করা হয়। বিক্রিয়াজাত পদার্থের মধ্যে উল্লেখযোগ্য পরিমানে ক্লোরিন যুক্ত বেনজোয়িক আ্যসিড ডেরিভেটিভ উপস্থিত থাকে। এই কারনে, মানুষের ব্যবহারের জন্য বেনজোয়িক আ্যসিড বেনজোয়েনের শুষ্ক পাতন থেকে পাওয়া যায়। ফুড-গ্রেড বেনজোয়িক আ্যসিড এখন সিন্থেটিকভাবে উৎপাদিত হয়।
ল্যাবরেটরিতে প্রস্তুতি
বেনজোয়িক আ্যসিড হল সস্তা এবং সহজলভ্য, তাই ল্যাবোরেটরিতে প্রস্তুত বেনজোয়িক আ্যসিড মূলত তার শিক্ষামানের জন্য অনুশীলন করা হয়। এটি একটি সাধারণ স্নাতক স্তরের প্রস্তুতি।
গরম জলে উচ্চ দ্রাব্যতা এবং ঠান্ডা জলে কম দ্রাব্যতার কারনে বেনজোয়িক আ্যসিড জল থেকে রিক্রিস্টালাইজেশন দ্বারা পরিশুদ্ধ করা যেতে পারে। রিক্রিস্টালাইজেশনের জন্য জৈব দ্রাবক ব্যবহার না করা এই পরীক্ষাটিকে বিশেষভাবে নিরাপদ করে তোলে। পদ্ধতিটি সাধারণত ৬৫% বিক্রিয়াজাত পদার্থ উৎপন্ন করে।
হাইড্রোলাইসিসের দ্বারা
ক্ষারীয় বা অম্লীয় (আ্যসিডিক) অবস্থায় অনান্য নাইট্রাইল এবং আ্যমাইড, বেনজোনাইট্রাইল এবং বেঞ্জামাইড এর মত যৌগগুলোকে বেনজোয়িক আ্যসিড বা তার কনজুগেট ক্ষারে হাইড্রোলাইজ করা যেতে পারে।
গ্রিগনার্ড বিকারক থেকে
ব্রোমোবেনজিনকে বেনজোয়িক আ্যসিডে রূপান্তরিত করা যেতে পারে অন্তর্বর্তী ফিনাইলম্যাগনেসিয়াম ব্রোমাইডের কার্বক্সিলেশন দ্বারা। এই পদ্ধতিটি গ্রিগনার্ড বিক্রিয়া চালানোর জন্য ছাত্রছাত্রীদের সুবিধাজনক অনুশীলন প্রদান করে, জৈব রসায়নে কার্বন-কার্বন বন্ধন তৈরির একটি গুরুত্বপূর্ণ বিক্রিয়া।
বেঞ্জাইল যৌগের অক্সিডেশন দ্বারা
বেনজাইল অ্যালকোহল এবং বেনজাইল ক্লোরাইড এবং কার্যত সব বেনজাইল ডেরিভেটিভগুলো খুব সহজে বেনজোয়িক আ্যসিডে রূপান্তরিত করা যায় অক্সিডেশন দ্বারা।
ব্যবহার
প্লাস্টিক তৈরিতে
ঔষধসম্বন্ধীয়
বেনজোয়িল ক্লোরাইড
ল্যাবরেটরিতে ব্যবহার
জীববিজ্ঞানে এবং স্বাস্থ্যে প্রভাব
বিক্রিয়াগুলো
আ্যরোমেটিক রিং
বেনজোইল গ্রুপ
নিরাপত্তা এবং স্তন্যপায়ী বিপাক
তথ্যসূত্র
- ↑ "Front Matter"। Nomenclature of Organic Chemistry : IUPAC Recommendations and Preferred Names 2013 (Blue Book)। Cambridge: The Royal Society of Chemistry। ২০১৪। পৃষ্ঠা 745। আইএসবিএন 978-0-85404-182-4। ডিওআই:10.1039/9781849733069-FP001।
- ↑ ক খ গ ঘ ঙ "benzoic acid"। chemister.ru। সংগ্রহের তারিখ ২৪ অক্টোবর ২০১৮।
- ↑ Seidell, Atherton; Linke, William F. (১৯৫২)। Solubilities of Inorganic and Organic Compounds। Van Nostrand। সংগ্রহের তারিখ ২০১৪-০৫-২৯।
- ↑ ক খ গ Benzoic acid in Linstrom, P.J.; Mallard, W.G. (eds.) NIST Chemistry WebBook, NIST Standard Reference Database Number 69. National Institute of Standards and Technology, Gaithersburg MD. http://webbook.nist.gov (retrieved 2014-05-23)
- ↑ Harris, Daniel (২০১০)। Quantitative Chemical Analysis (8 সংস্করণ)। New York: W. H. Freeman and Company। পৃষ্ঠা AP12। আইএসবিএন 9781429254366।
- ↑ Olmstead, William N.; Bordwell, Frederick G. (১৯৮০)। "Ion-pair association constants in dimethyl sulfoxide"। The Journal of Organic Chemistry। 45 (16): 3299–3305। ডিওআই:10.1021/jo01304a033।
- ↑ ক খ গ ঘ Record in the GESTIS Substance Database from the IFA
- ↑ ক খ গ Sigma-Aldrich Co. Retrieved on 2014-05-23.