পটাশিয়াম পারম্যাঙ্গানেট
রাসায়নিক যৌগ
(পটাসিয়াম পারম্যাঙ্গানেট থেকে পুনর্নির্দেশিত)
এই নিবন্ধটি ইংরেজি উইকিপিডিয়ার অনুরূপ নিবন্ধ অনুবাদ করে সম্প্রসারণ করা যেতে পারে। (সেপ্টেম্বর ২০২২) অনুবাদ করার আগে গুরুত্বপূর্ণ নির্দেশাবলী পড়ার জন্য [দেখান] ক্লিক করুন।
|
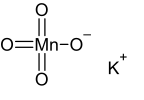
পটাশিয়াম পারম্যাঙ্গানেট হচ্ছে অজৈব যৌগ যার রাসায়নিক সংকেত KMnO4 এবং K+ ও MnO−
4 দ্বারা গঠিত. এটা লালচে কালো স্ফটিকাকার কঠিন পদার্থ, যেটি পানিতে দ্রবীভূত হয়ে তাৎক্ষণিক গোলাপি বা লালচে দ্রবণ তৈরি করে। [তথ্যসূত্র প্রয়োজন]
| |
| |

| |
| নামসমূহ | |
|---|---|
| ইউপ্যাক নাম
পটাশিয়াম পারম্যাঙ্গানেট (VII)
| |
| অন্যান্য নাম
পটাশিয়াম পারম্যাঙ্গানেট
বহুরূপী খনিজ কন্ডির স্ফটিক পটাশ এর পারম্যাঙ্গানেট হাইপারম্যাঙ্গন | |
| শনাক্তকারী | |
ত্রিমাত্রিক মডেল (জেমল)
|
|
| সিএইচইএমবিএল | |
| কেমস্পাইডার | |
| ড্রাগব্যাংক | |
| ইসিএইচএ ইনফোকার্ড | ১০০.০২৮.৮৭৪ |
| ইসি-নম্বর |
|
| কেইজিজি | |
পাবকেম CID
|
|
| আরটিইসিএস নম্বর |
|
| ইউএনআইআই | |
| ইউএন নম্বর | 1490 |
কম্পটক্স ড্যাশবোর্ড (EPA)
|
|
| |
| |
| বৈশিষ্ট্য | |
| KMnO4 | |
| আণবিক ভর | 158.034 g/mol |
| বর্ণ | লালচে ধূসর দ্রবণে গোলাপী ম্যাজেন্টা[১] |
| গন্ধ | গন্ধ বিহীন |
| ঘনত্ব | ২.৭ গ্রাম/সেমি৩ [২]:৪.৮৩ |
| গলনাঙ্ক | ২৪০ °সে (৪৬৪ °ফা; ৫১৩ K) (decomposes) |
| ৭৬ গ্রাম/লিটার (২৫ °C)[২] ২৫০ গ্রাম/লিটার (৬৫ °C) | |
| দ্রাব্যতা | অ্যালকোহল এবং জৈবযৌগে দ্রবীভূত |
| +২০.০·১০−৬ সেমি৩/মোল[২]:৪.১৩৪ | |
| প্রতিসরাঙ্ক (nD) | ১.৫৯ |
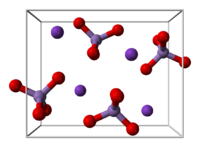
| গঠন[৩] | |
| স্ফটিক গঠন | Orthorhombic, oP24 |
| Space group | Pnma, No. 62 |
| Lattice constant | |
এককের সূত্রসমূহ (Z)
|
4 |
| তাপ রসায়নবিদ্যা | |
| তাপ ধারকত্ব, C | 119.2 J/mol K |
| স্ট্যন্ডার্ড মোলার এন্ট্রোফি এস |
171.7 J K−1 mol−1 |
| গঠনে প্রমান এনথ্যাল্পির পরিবর্তন ΔfH |
−813.4 kJ/mol |
গিবসের মুক্ত শক্তি (ΔfG˚)
|
-713.8 kJ/mol |
| ঔষধসংক্রান্ত | |
| ATC code | |
| ঝুঁকি প্রবণতা | |
| জিএইচএস চিত্রলিপি |   
|
| এনএফপিএ ৭০৪ | |
| প্রাণঘাতী ডোজ বা একাগ্রতা (LD, LC): | |
LD৫০ (মধ্যমা ডোজ)
|
1090 mg/kg (oral, rat)[৪] |
| সম্পর্কিত যৌগ | |
অন্যান্য অ্যানায়নসমূহ
|
Potassium manganate |
অন্যান্য ক্যাটায়নসমূহ
|
Sodium permanganate Ammonium permanganate Calcium permanganate Silver permanganate |
সম্পর্কিত যৌগ
|
Manganese heptoxide |
সুনির্দিষ্টভাবে উল্লেখ করা ছাড়া, পদার্থসমূহের সকল তথ্য-উপাত্তসমূহ তাদের প্রমাণ অবস্থা (২৫ °সে (৭৭ °ফা), ১০০ kPa) অনুসারে দেওয়া হয়েছে। | |
| তথ্যছক তথ্যসূত্র | |
পটাশিয়াম পারম্যাঙ্গানেট রাসায়নিক শিল্পে এবং ল্যাবরেটরিতে তীব্র জারক পদার্থ হিসেবে ব্যাপকভাবে ব্যবহৃত হয়। চর্মরোগের চিকিৎসা দ্রব্য, ক্ষত পরিষ্কার করতে, ও সাধারণ জীবানুনাশক হিসেবে এর ব্যবহার রয়েছে. এটা WHO কর্তৃক প্রয়োজনীয় ওষুধ হিসেবে স্বীকৃত এবং স্বাস্থ্য ক্ষেত্রে অত্যধিক কার্যকরী ও নিরাপদ ঔষধ। [৫] ২০০০ সালে, বিশ্বব্যাপী উৎপাদন অনুমানিক ৩০,০০০ টন।[তথ্যসূত্র প্রয়োজন]
ব্যবহার সম্পাদনা
ইতিহাস সম্পাদনা
প্রস্তুতি সম্পাদনা
গঠন সম্পাদনা
বিক্রিয়া সম্পাদনা
নিরাপত্তা সম্পাদনা
তথ্যসূত্র সম্পাদনা
- ↑ Burriel, F.; Lucena, F.; Arribas, S. and Hernández, J. (1985), Química Analítica Cualitativa, p. 688, আইএসবিএন ৮৪-৯৭৩২-১৪০-৫.
- ↑ ক খ গ Haynes, William M., সম্পাদক (২০১১)। CRC Handbook of Chemistry and Physics (92nd সংস্করণ)। CRC Press। আইএসবিএন 978-1439855119।
- ↑ Hocart R., Sicaud, Mathieu (1945) C R Hebd Seances Acad Sci., 221, 261–263
- ↑ Chambers, Michael। "ChemIDplus – 7722-64-7 – VZJVWSHVAAUDKD-UHFFFAOYSA-N – Potassium permanganate [USP:JAN] – Similar structures search, synonyms, formulas, resource links, and other chemical information."। chem.sis.nlm.nih.gov। ১৩ আগস্ট ২০১৪ তারিখে মূল থেকে আর্কাইভ করা। সংগ্রহের তারিখ ৯ মে ২০১৮।
- ↑ World Health Organization (২০১৯)। World Health Organization model list of essential medicines: 21st list 2019। Geneva: World Health Organization। hdl:10665/325771 । WHO/MVP/EMP/IAU/2019.06. License: CC BY-NC-SA 3.0 IGO।
বহিঃসংযোগ সম্পাদনা
- আন্তর্জাতিক রাসায়নিক নিরাপত্তা কার্ড 0672
- "Potassium permanganate"। Drug Information Portal। U.S. National Library of Medicine।
- National Pollutant Inventory: Manganese and compounds Fact Sheet
- The use of potassium permanganate in fish ponds
